Atomos
Tenemos que empezar con un poco de química porque los organismos vivos están hechos de y el uso de productos químicos.
Sustancias individuales se denominan elementos , sustancia que no se puede romper o subdividida por medios químicos ordinarios. Reconocemos unos 105 o 106 elementos. Alrededor del 92 son naturales y el resto son hechos por el hombre. Estas son cosas como oxígeno, azufre, carbón, cobre, etc Cada elemento tiene un símbolo hecho de las primeras letras de su nombre. Algunos son de los viejos nombres en latín: sodio = natrium, hierro = ferrum, potasio = kalium. Del 92 de origen natural, cuatro de ellos representan alrededor del 96% de toda la materia viva. Estos son carbono, oxígeno, hidrógeno y nitrógeno, y el nombre COHN puede ayudarle a recordar estos. Otro 21 son necesarios en cantidades más pequeñas con el fin de vivir y mantenerse sano.
Una sola pieza, una partícula de un elemento es un átomo de una unidad de materia o de la cantidad más pequeña posible de un elemento. Dos o más átomos pueden unirse entre sí para formar una molécula . A menudo, el compuesto formado de este modo tiene propiedades muy diferentes de los elementos en el mismo. Por ejemplo, sodio (Na), una, de metal casi explosivo extremadamente reactivo, y cloro (Cl), un gas tóxico se combinan para formar cloruro de sodio (NaCl), que es la sal de mesa común.
Los átomos están formados por las cosas aún más pequeñas llamadas partículas subatómicas . Hay tres tipos principales: de protones (que tiene una muy pequeña carga eléctrica positiva), neutrones (que es neutro), y de electrones (que tiene una muy pequeña carga eléctrica, negativa). Usted puede ver estos denominado p + , e - y n o . Los protones y los neutrones forman el núcleo del átomo (que no debe confundirse con el núcleo de una célula), mientras que los electrones están dando vueltas en algún lugar y viajan aproximadamente a la velocidad de la luz.
El número de protones es importante: esto determina qué elemento es algo. Cada elemento tiene un número diferente de protones, y si el número de protones en un átomo cambia, entonces qué elemento es. El número de protones en un átomo se llama su número atómico . Esto se escribe como subíndice a la izquierda: 8 O, 6 C, etc
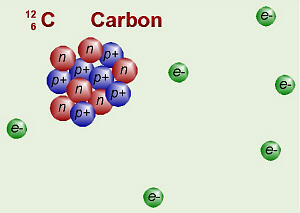
Dentro de ciertos límites, el número de neutrones y electrones en un átomo puede variar. Isótopos son átomos de un mismo elemento con diferente número de neutrones.Los protones y los neutrones pesan casi lo mismo que los demás, pero los electrones son mucho más pequeños, su peso es insignificante en comparación (como llevar una pluma cuando usted se pesa en la balanza de baño). Por lo tanto, cuando queremos saber cuánto pesa un átomo de algo, podemos simplemente sumar el número de protones y neutrones. El número de protones más el número de neutrones en un átomo = su peso atómico . Estos son escritos como superíndices a la izquierda: 12 C, 13C El peso atómico menos el número atómico es igual al número de neutrones. Esto significa que el carbono-12 tiene 6 neutrones, el carbono-13 tiene 7, y carbono-14 ha 8. En carbono-14, la relación de neutrones a protones (8 a 6) es lo suficientemente lejos de que el núcleo del átomo no es estable, pero se somete a la desintegración radiactiva , en el que se convierte en algún otro producto químico (más allá del alcance de este curso , pero si usted está interesado, la reacción radiactivo real, llamado
nivel de emisiones, es 6 14 C 7 14 N + e - , y el electrón que está "echado" se llama beta [ ] de partículas). La vida media de un químico radioactivo es la cantidad de tiempo que tarda la mitad de la cantidad de partida para someterse a la desintegración radiactiva. Por lo tanto, si usted empieza con 1 g de una sustancia con una vida media de 1 año, después de un año, tendría 0,5 gm izquierdo, después de dos años que tendría sólo 0,25 g, después de tres años, 0.125, etc 

Peso molecular es igual a la suma de los pesos atómicos de los átomos en la molécula. Para NaCl, el peso atómico del sodio es 23, de cloro es 35 y una molécula contiene uno de sodio y uno de cloro, por lo que 23 + 35 = 58, el peso molecular de NaCl. La fórmula para la glucosa (un azúcar muy común) es C 6 H 12 O 6 . Los subíndices a la derecha significan que contiene 6 átomos de carbono, 12 átomos de hidrógeno, y 6 átomos de oxígeno. El peso atómico de carbono es 12, para el hidrógeno es 1, y para el oxígeno es 16, por lo que el peso molecular de la glucosa se puede calcular así:
Utilice la Tabla Periódica de abajo para ayudarle con este problema en la práctica el peso molecular . (Obtendrás un problema diferente cada vez que haga clic en este enlace.)
Los números vamos a ver que aparecen en la tabla periódica son promedios, por ejemplo, para el carbono del número dado es un peso atómico promedio de todo el carbono-12, carbono-13 y carbono-14 en el mundo.Para nuestros propósitos, no pasa nada si se redondea al número entero más próximo (C = 12, S = 16).
Normalmente, el número de protones y electrones coincide con lo que la carga se equilibra. A veces, sin embargo, el número de electrones puede variar. Los iones son átomos con electrones añadidos o eliminados que resulta en una carga global positiva o negativa. En general, la carga de un ion se indica a la parte superior derecha de su símbolo. Por ejemplo, un ión de calcio con una carga 2 se indicaría como Ca + + o Ca 2 . Los electrones se mueven rápidamente alrededor del átomo, y pueden tener ciertas cantidades discretas de energía (como hacer el cambio en el que pueda tener ya sea un centavo o un centavo o un centavo, pero no una moneda de ¢ 3.5). Estas cantidades se refieren como conchas de energía o orbitales. Estos no son órbitas como los planetas alrededor del sol, sino un intento de mostrar las cantidades de energía que cuadros.
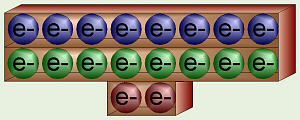
Cada cantidad de energía / nivel / shell solo pueden tener un cierto número de electrones con la energía mucho, algo así como si usted va a una película en la que hay 1, 5 y 10 escaños ¢. El primer nivel de energía puede tener dos electrones (hay dos asientos 1 ¢). Si hay más electrones, deben tener la siguiente cantidad de energía (que tienen que comprar 5 asientos ¢), o como un químico diría que están llenando la segunda capa de energía. Ocho electrones pueden tener el segundo nivel de energía (ocho asientos 5 ¢). Si todavía hay más electrones de los átomos de un elemento en particular, entonces deben ir a la tercera capa de energía (comprar 10 escaños ¢) donde hay otros ocho lugares disponibles. Más allá de eso, las cosas se complican mucho la biología, así que lo dejo a los químicos.
Los químicos, sin embargo, prefieren no pensar en términos de 1, 5, y 10 escaños ¢ en una película. A menudo, los orbitales / conchas de energía se representan como círculos alrededor del centro del átomo. Una vez más, los electrones no viajan en torno a estos círculos como los planetas. Más bien, esto es sólo una forma de mostrar la cantidad de energía que tienen. Nuestros asientos de cine convertirían a orbitales algo como esto "estándar".
Así es como un químico haría diagrama de los niveles de energía de este átomo. Tenga en cuenta que los electrones vienen en pares . Esta idea es importante para mostrar cómo bond átomos entre sí para formar moléculas. Por lo tanto, el primer nivel de energía puede tener un par de electrones, el segundo nivel puede tener cuatro pares, etc
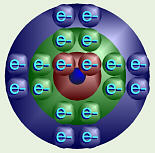
Como átomos de diferentes elementos de ganancia de un número creciente de electrones, uno se pone en cada par en un nivel antes de que el segundo "medio" de cada par está lleno. Por lo tanto, para el carbono, con seis protones y seis electrones, dos de los electrones llenan el par disponible en la primera capa de energía. Los cuatro electrones restantes se distribuyen, uno en cada uno de los cuatro pares en el segundo nivel.
Los electrones gustaría tener la menor cantidad de energía posible, por lo que estos niveles se llenan "de abajo hacia arriba" (todos ellos llenan los asientos baratos primero), por lo que no todos los átomos tienen electrones en todos los depósitos. El número de electrones en cada una de las conchas depende de la cantidad total de electrones que tienen. Este número es generalmente el mismo que el número de protones debido a que la carga eléctrica de un electrón es igual pero opuesta a la de un protón. Por lo tanto, el hidrógeno tiene un electrón en el primer nivel, el helio tiene dos en el primer nivel, el litio tiene las dos de la primera y uno en el segundo nivel, etc Tenga en cuenta la disposición de la tabla periódica: elementos están organizados en columnas por el número de electrones que tienen en sus niveles de energía más externos (por ejemplo, H, Li, Na y cada uno tiene un electrón en cualquier nivel de energía es "externa"), y se organizan en filas en que el nivel de energía (1 ª , 2 ª , etc) que están de relleno (por ejemplo, Li, C y N tienen su primer nivel de energía total y se encuentran en distintas etapas / número de electrones de llenar su segundo nivel).

Para cualquier elemento, los electrones en el nivel de energía más externo / shell son los más importantes. Estos determinan las propiedades químicas de un elemento - cómo va a reaccionar en una reacción química. Estos electrones importantes se conocen como los electrones de valencia . Saber el número de electrones de valencia de carbono, oxígeno, hidrógeno, nitrógeno, sodio, cloro y tienen.
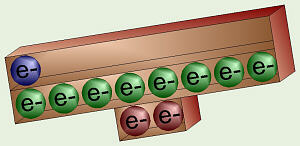
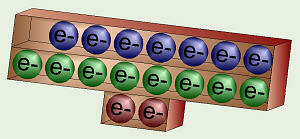
Todos los elementos son más estables, con un nivel de energía externa completa, lo que ese nivel es, por lo que ganar o ceder electrones para hacer todo lo que es el nivel más externo sea completo, incluso si no coincide con el número de protones en un átomo. Esto sería un ión , y si el átomo de ganado electrones para formar un ion (hay más electrones que protones), a continuación, sería su carga eléctrica negativa general por sin embargo muchos electrones "extra" que tiene. Si un átomo cede electrones para formar un ion (hay más protones que electrones), entonces su carga global es positiva.
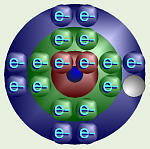
Considere la posibilidad de sodio y cloro. Sodio se encuentra en la columna que lo que tiene un electrón de valencia. Si se pudiera librarse de aquel, electrón solitario desde el nivel 3, entonces su nivel externo sería el nivel 2, que es bueno y completo. El cloro se encuentra en la columna VII, por lo que tiene siete electrones de valencia, uno menos que una cáscara externa completa. Por lo tanto, sería más estable si se pudiera tomar un electrón de un lugar para llenar hasta que uno, último lugar.
Moleculas de agua
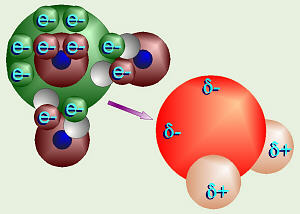
La forma de una molécula de agua es también un tetraedro. El oxígeno tiene seis electrones de valencia y dos "agujeros", por lo tanto puede enlazar con dos hidrógenos.Por lo tanto, la fórmula química del agua es H 2 O. Otros cuatro electrones de valencia del oxígeno, en dos pares, no se unen a ningún otro átomo, por lo tanto estos se conocen como pares de electrones no compartidos . Acciones de oxígeno con los electrones de hidrógeno, pero jala un poco más difícil para los electrones. Los electrones son sólo un poco más cerca del oxígeno que los átomos de hidrógeno, por lo que se denomina enlace covalente polar . Tenga en cuenta que a pesar de que la molécula en su conjunto es eléctricamente neutro (el cargas + y - el equilibrio), los extremos de la molécula donde los núcleos de hidrógeno son (que contienen sólo un protón) tienen una carga positiva de tipo-, y los extremos de los la molécula por los pares de electrones no compartidos son una especie de negativo. Los extremos especie de positivos en una molécula de agua se sienten atraídos por el estilo-de extremos negativos sobre otra molécula de agua. Esto se denomina enlace de hidrógeno . En realidad, el enlace de hidrógeno puede ocurrir con otras moléculas, además de agua, como veremos más adelante.
El agua es un ingrediente clave para la vida. Las células son 70 a 95% de agua. Alrededor del 75% de la superficie terrestre está cubierta de agua. El agua es la única sustancia común que existe de manera natural en las tres formas: sólido, líquido o gas. El agua tiene muchas propiedades únicas debido, en gran parte, a su enlace de hidrógeno.
PH
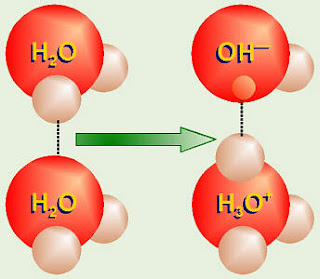
Incluso en, agua destilada normal, debido a la unión de hidrógeno, a veces uno de los protones de hidrógeno de una molécula de agua "salta" a uno de los pares de electrones no compartidos en otra molécula de agua (dejando detrás de su electrón). Así iones H 3 O + (ion hidronio) y OH - se forman (iones hidróxido). Esta reacción se puede escribir como 2 H 2 O  H 3 O + + OH - . Alguien descubrió que en un litro de agua destilada pura, habrá 0.0000001 M cada uno de H 3 O +(escrito a menudo como H + ) y de OH - presente.
H 3 O + + OH - . Alguien descubrió que en un litro de agua destilada pura, habrá 0.0000001 M cada uno de H 3 O +(escrito a menudo como H + ) y de OH - presente.
 H 3 O + + OH - . Alguien descubrió que en un litro de agua destilada pura, habrá 0.0000001 M cada uno de H 3 O +(escrito a menudo como H + ) y de OH - presente.
H 3 O + + OH - . Alguien descubrió que en un litro de agua destilada pura, habrá 0.0000001 M cada uno de H 3 O +(escrito a menudo como H + ) y de OH - presente.
En lugar de tener que escribir todo eso, los químicos se le ocurrió el concepto de pH como una forma abreviada para realizar un seguimiento de la cantidad de H 3 O + está presente en una solución. En primer lugar, la 0.0000001 M se convierte a notación científica, por lo que se convierte en 1 × 10 -7 . A continuación, el exponente o logaritmo de ese número se encuentra: el logaritmo de 1 × 10 -7 es simplemente -7. Entonces, ya que los científicos, al igual que otras personas, no me gusta tener que hacer nada más escrito de lo necesario, lo negativo - se retira signo (). En base a todo esto, pH =-log [H + ] , o el pH es igual al logaritmo negativo de la de hidrógeno (hidronio) la concentración de iones (" [] "medios" la concentración de ").
Si se añaden otras sustancias, las concentraciones de hidrógeno (hidronio) y iones de hidróxido (anotada como [H + ] y [OH - ]) pueden cambiar, pero el pH siempre se basa en la concentración de iones de hidrógeno, [H + ]. Si [H + ] es mayor que 0,0000001 M, (como 0,0001 o 10 -4 pH so = 4), que la solución es un ácido, y si [H + ] es menor que 0,0000001 M, (como 0,0000000001 ó 10 -10 para pH = 10) la solución es una base. Alguien descubrió que [H + ] × [OH - ] siempre es igual a 10 -14 , por lo que si uno aumenta, la otra disminuye, proporcionalmente, de tal manera que el producto de los dos será siempre 10 -14 .
Pruebe con un problema de la práctica pH . (Obtendrás un problema diferente cada vez que haga clic en este enlace.)
Un ácido es una sustancia que se añade H + a una solución. Una de base es una sustancia que resta H + desde o añade OH - a una solución. Una solución neutra tiene un pH de 7. Si el pH de una solución es inferior a 7 (porque [H + ] es mayor que 10 -7 ) la solución es un ácido, y si el pH es mayor que 7 (porque [H + ] es menor que 10 -7 ) la solución es una base. Las sustancias biológicas como el jugo de limón y el vinagre son ácidos, y ambos tienen valores de pH alrededor de 3. El ácido clorhídrico (HCl) en el limpiador de inodoro y en el estómago es un ácido fuerte - el pH ácido del estómago es de entre 1 y 3. Lejía (NaOH), el ingrediente principal en muchos drenaje-abridores, es una base fuerte, con un pH de 12 a 14, dependiendo de la concentración de la solución. He oído que el pH típico de nuestro cuero cabelludo y la piel es de alrededor de 5, ligeramente ácido y pH que es mejor para la piel y el cuero cabelludo de la salud y la resistencia a las infecciones y enfermedades. Jabón y muchos champús se realizan a través de una reacción química que implica la lejía, y puesto que no suele ser un poco de lejía sin reaccionar que queda en ellos, son bases (algunas bases muy fuertes). Por lo tanto, mientras que nuestra piel puede secretar productos químicos para recuperar su equilibrio del pH después de vez en cuando, el uso razonable de estos productos, el uso demasiado frecuente de estos productos (lavado con champú el cabello sobre una base diaria, duchas diarias utilizando jabón o barras de detergente) pueden prevenir el cuero cabelludo / piel de mantener un pH normal, lo que resulta en (= menos saludables) piel "seca" y un mayor riesgo de infección. Por lo tanto, algunos fabricantes de champú añaden productos químicos a sus champús para bajar el pH cerca de lo normal de la piel de pH 5, y estos champús a menudo se comercializan como champús "pH-equilibrados". He escuchado a personas bien informadas, incluidos los dermatólogos, dicen que es mejor para la piel de uno de no tomar duchas diarias, o al menos a no usar jabón (sólo enjuague con agua) si alguien siente que una ducha diaria es un "must". ( Curiosamente, aunque no he visto estudios científicos reales sobre esto, he oído / leído que nuestro cuero cabelludo segrega sustancias químicas que ayudan a repeler los piojos, y la sugerencia de que el aumento de la incidencia de piojos entre los escolares de nuestro país puede, en parte, , se relaciona con el hecho de que los padres son en realidad mantener el cabello de sus hijos "demasiado limpio", evitando así la acumulación de una cantidad adecuada de repelente natural de su cabello.)
Un tampón es una sustancia que reduce al mínimo el cambio en el pH o [H + ]. Diferentes tampones funcionan mejor en diferentes intervalos de pH. Tenga en cuenta que lo que está sucediendo aquí es que un amortiguador protege demasiado grande de un cambio en el pH. De ninguna manera es esto algo así como el equivalente de la reducción / minimización del pH, lo que tendría el efecto de crear un ácido fuerte. El concepto de pH y la utilización de tampones para mantener rangos de pH "normales" son importantes en nuestros cuerpos y en otras ramas de la biología. Por ejemplo, una enzima llamada pepsina digiere las proteínas en el estómago, pero debe tener un entorno ácido para la función (la mayoría de las enzimas en nuestros cuerpos funcionar sólo dentro de ciertos rangos de pH). No todos los alimentos que consumimos es ácida, y puede destruir (o neutralizar) el pH normal del estómago, con lo que la pepsina ineficaz, incapaz de digerir la proteína de la dieta. Para evitar que esto suceda, los tampones en nuestro estómago mantener el pH bastante constante, dentro de un intervalo de aproximadamente pH 1 a 3. Sin embargo, los antiácidos como Tums ® o Rolaids ® son tan "fuerte" que abruman la capacidad de buffers de estómago de la persona "para que funcione correctamente, cambiando drásticamente el pH del contenido del estómago, y por lo tanto, la capacidad de pepsina para digerir la proteína en la dieta. El calcio, por cierto, se absorbe mejor en el cuerpo de uno si los contenidos del estómago son ácidos, por lo que los antiácidos también interfieren con la capacidad de nuestro cuerpo para absorber adecuadamente el calcio. Para absorber correctamente el calcio en la dieta, que debe ser consumido junto con sustancias ácidas o ligeramente ácido (tales como leche o jugo de naranja), y no se mezcla con antiácidos. Si bien puede haber un uso legítimo de antiácidos (como cuando un médico le receta para ayudar en el tratamiento de las úlceras), el uso "casual" frecuente de antiácidos puede llegar a estimular la producción de más ácido estomacal como el sistema del usuario se esfuerza por superarlos y volver el cuerpo a la normalidad. Como otro ejemplo, la sangre debe permanecer muy cerca de alrededor de pH 7,4, y si se desvía demasiado, una persona puede enfermarse gravemente o morir. Sin embargo, cuando nos transportamos dióxido de carbono de las células a los pulmones, se convierte en ácido carbónico en la sangre desoxigenada. Por lo tanto, si no fuera por tampones, nuestra sangre sería un pH drásticamente diferente dependiendo de la cantidad de dióxido de carbono se disuelve en ella.

No hay comentarios :
Publicar un comentario